Lần đầu chỉnh sửa gene trực tiếp trên người
- Chủ nhật - 08/03/2020 17:37
- |In ra
- |Đóng cửa sổ này
 |
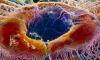
| Cấu tạo võng mạc của người. Ảnh: Nature. |
Các nhà khoa học lần đầu tiên sử dụng phương pháp chỉnh sửa gene CRISPR-Cas9 trực tiếp trên cơ thể một người mắc bệnh mù bẩm sinh Leber 10 (LCA10), Nature hôm 5/3 đưa tin. Đây là một phần trong BRILLIANCE, cuộc thử nghiệm lâm sàng quan trọng nhằm kiểm tra khả năng loại bỏ các đột biến gây LCA10 của CRISPR-Cas9. LCA10 là căn bệnh khiến trẻ em mất thị lực và hiện chưa có cách chữa trị.
Trong lần thử nghiệm mới, những bộ phận của công cụ chỉnh sửa gene được truyền trực tiếp vào mắt, gần các tế bào cảm nhận ánh sáng. Trong những thử nghiệm lâm sàng trước đó, các chuyên gia chỉ chỉnh sửa bộ gene của tế bào đã tách ra ngoài, sau đó đưa lại vào cơ thể bệnh nhân.
"Đây là một thử nghiệm thú vị", Mark Pennesi, chuyên gia về bệnh võng mạc tại Đại học Khoa học & Y tế Oregon, nhận định. Pennesi đang hợp tác với công ty dược Editas Medicine và Allergan để tiến hành BRILLIANCE.
Đây không phải lần đầu tiên giới chuyên gia sử dụng kỹ thuật chỉnh sửa gene trên người. Nuclease ngón tay kẽm (ZFN), một phương pháp chỉnh sửa gene cũ hơn, từng được áp dụng trực tiếp trên cơ thể người tham gia thử nghiệm lâm sàng. Công ty Sangamo Therapeutics đã thử điều trị hội chứng Hunter bằng phương pháp này. Theo đó, bản sao khỏe mạnh của gene bị ảnh hưởng được đặt vào một vị trí cụ thể trong bộ gene của các tế bào gan. Dù có vẻ an toàn, kết quả sơ bộ cho thấy có thể cách này không mấy hiệu quả trong việc loại bỏ các triệu chứng của hội chứng Hunter.
Với BRILLIANCE, lần đầu tiên các nhà khoa học sử dụng kỹ thuật CRISPR-Cas9, vốn được khen ngợi là linh hoạt, trực tiếp trên cơ thể người. Kỹ thuật này giúp họ loại bỏ một đột biến trong gene CEP290 gây ra LCA10.
Theo cách truyền thống, các chuyên gia sẽ đưa bản sao khỏe mạnh của gene đột biến vào trong các tế bào bị ảnh hưởng thông qua một virus. Tuy nhiên, CEP290 quá lớn nên không thể đưa vào bộ gene của virus, theo Artur Cideciyan, chuyên gia nghiên cứu bệnh võng mạc tại Đại học Pennsylvania.
Với người mắc LCA10, các tế bào cảm nhận ánh sáng trong võng mạc bị đột biến ở CEP290 vô hiệu hóa. Tuy nhiên, chúng vẫn còn tồn tại. "Chúng tôi hy vọng có thể tái kích hoạt những tế bào đó. Đây là một trong số ít những bệnh mà chúng tôi nghĩ bệnh nhân có thể cải thiện thị lực", Pennesi nói.
Kết quả ban đầu của một phương pháp chữa trị khác cho thấy điều này có thể khả thi. Phòng thí nghiệm Cideciyan hợp tác với công ty ProQR để điều trị bệnh nhân LCA10 bằng phương pháp thử nghiệm mang tên sepofarsen. Sepofarsen sử dụng kỹ thuật đối mã để sửa lại đột biến trong ARN gây ra LCA10 từ gene CEP290. Kết quả ban đầu cho thấy phương pháp này có thể cải thiện thị lực của bệnh nhân.
Sử dụng CRISPR-Cas9 trên cơ thể người là bước đột phá từ việc điều trị tế bào trong đĩa thí nghiệm, theo Fyodor Urnov, chuyên gia nghiên cứu kỹ thuật chỉnh sửa gene tại Đại học California. "Điều này giống như so sánh một chuyến du hành vũ trụ với chuyến bay bằng máy bay thông thường. Những thách thức về kỹ thuật và lo ngại về độ an toàn cũng nhiều hơn", Urnov chia sẻ.